大肠菌群(Coliform bacteria)是指一群能发酵乳糖、产酸产气、需氧和兼性厌氧的革兰氏阴性无芽胞杆菌。该菌主要来源于人畜粪便,故以此作为粪便污染指标来评价食品的卫生质量,推断食品中是否有污染肠道致病菌的可能。大肠菌群分布较广,在温血动物粪便和自然界中广泛存在。
调查研究表明,大肠菌群多存在于温血动物粪便、人类经常活动的场所以及有粪便污染的地方。人、畜粪便对外界环境的污染是大肠菌群在自然界存在的主要原因之一,粪便中多以典型大肠杆菌为主,而外界环境中则大肠菌群的其他菌株较多。
一、检测方法
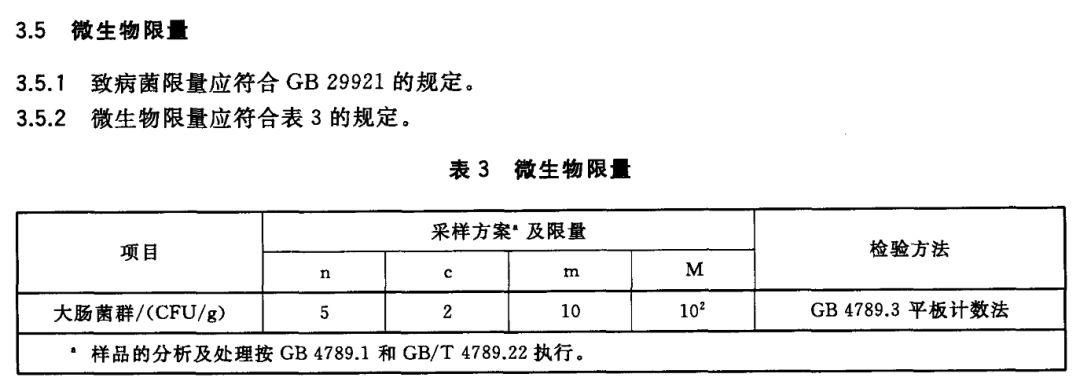
大肠菌群检测的关键在于方法的选用,食品中大肠菌群检测有两种表示方法,其一是以100mL(g)检样内大肠菌群最大可能数(MPN)表示,检测方法需使用GB/T 4789.3-2003《食品卫生微生物学检验大肠菌群测定》;
其二以每g(mL)样品中大肠菌群的MPN值表示,检测方法需使用GB 4789.3-2016《食品安全国家标准 食品微生物学检验 大肠菌群计数》。GB/T 4789.3-2003《食品卫生微生物学检验 大肠菌群测定》虽然被后更新的方法代替,但卫生部关于规范食品中大肠菌群指标的检测工作公告(2009年 第16号)明确指出,为规范食品中大肠菌群指标的检测工作公告如下:
现行食品标准中规定的大肠菌群指标以“MPN/100克或MPN/100毫升”为单位的,适用《食品卫生微生物学检验大肠菌群测定》(GB/T 4789.3-2003)进行检测;
以“MPN/克或MPN/毫升”、“CFU/克或CFU/毫升”为单位的,适用《食品卫生微生物学检验大肠菌群计数》(GB/4789.3-2016)进行检测。
例如,GB/T2717-2003酱油卫生标准中对大肠菌群的要求需使用方法一GB/T 4789.3-2003。又如GB/T 2718-2014酱油卫生标准中对大肠菌群的要求需使用方法二GB4789.3-2016。

MPN检索表使用:GB/T 4789.3-2003检索表中阳性管数是以1mL(g)×3、0.1mL(g)×3和0.01mL(g)×3的梯度进行表示,GB 4789.3-2016阳性管数是以0.10、0.01和0.001的梯度表示,均按照稀释倍数推算结果,结果相同。推算方法以GB 4789.3-2016为例,改用1g(mL)、0.1g(mL)和0.01g(mL)时,表内数字应相应降低10倍;如改用0.01g(mL)、0.001g(mL)和0.0001g(mL)时,则表内数字应相应增高10倍,其余类推即可。
二、常用标准
1、 GB/T 4789.3-2003 食品卫生微生物学检验 大肠菌群测定;
2、GB 4789.3-2016 食品安全国家标准 食品微生物学检验 大肠菌群计数;
3、GB 4789.28-2013 食品安全国家标准 食品微生物学检验 培养基和试剂的质量要求;
4、GB 4789.1-2016 食品安全国家标准 食品微生物学检验 总则;
5、GB 4789.41-2016 食品安全国家标准 食品微生物学检验 肠杆科检验;
6、GB/T 27405-2008 实验室质量控制规范 食品微生物检测7、GB/T 16294-2010 医药工业洁净室(区) 沉降菌的测试方法。
三、常见问题及解答
1、食品中大肠菌群的检测有两个标准三种方法,该如何选择呢?
A:依据产品标准的项目单位
若单位为CFU/g,则选择GB 4789.3-2016第二法(平板计数法)
若单位为MPN/g,则选择GB 4789.3-2016第一法(MPN计数法)
若单位为MPN/100g,则选择GB/T 4789.3-2003。
2、MPN法3个适宜的连续稀释度该怎样选择?A:依据产品标准的项目标准值
若标准值为<3.0MPN/g,则选择0.1g、0.01g、0.001g三个稀释度。
若标准值为≤30MPN/100g,则选择1g、0.1g、0.01g三个稀释度。
四、样品采集
怎样采样,才能使样品具有代表性?
这里将样品分为两类:预包装食品和散装食品或现场制作食品:
1、对于预包装食品
①应采集相同批次、独立包装、适量件数的食品样品,每件样品的采样量应满足微生物项目检验的要求。
②独立包装小于、等于1000g 的固态食品或小于、等于1000mL 的液态食品,取相同批次的包装。
③独立包装大于1000mL 的液态食品,应在采样前摇动或用无菌棒搅拌液体,使其达到均质后采集适量样品,放入同一个无菌采样容器内作为一件食品样品;大于1000g 的固态食品,应用无菌采样器从同一包装的不同部位分别采取适量样品,放入同一个无菌采样容器内作为一件食品样品。
2、对于散装食品或现场制作食品用无菌采样工具从n个不同部位现场采集样品,放入n个无菌采样容器内作为n件食品样品。每件样品的采样量应满足微生物项目检验单位的要求。怎样采样,才能使样品具有代表性?
这里将样品分为两类:预包装食品和散装食品或现场制作食品。
1、对于预包装食品
①应采集相同批次、独立包装、适量件数的食品样品,每件样品的采样量应满足微生物项目检验的要求。
②独立包装小于、等于1000g的固态食品或小于、等于1000mL的液态食品,取相同批次的包装。
③独立包装大于1000mL的液态食品,应在采样前摇动或用无菌棒搅拌液体,使其达到均质后采集适量样品,放入同一个无菌采样容器内作为一件食品样品;大于1000g的固态食品,应用无菌采样器从同一包装的不同部位分别采取适量样品,放入同一个无菌采样容器内作为一件食品样品。
2、对于散装食品或现场制作食品用无菌采样工具从n个不同部位现场采集样品,放入n个无菌采样容器内作为n件食品样品。每件样品的采样量应满足微生物项目检验单位的要求。
五、培养基制备过程容易出现问题解答
1、异常现象一:培养基不凝固
原因分析:
①制备过程中过度加热;
②低pH造成培养基酸解;
③称量不正确;
④琼脂未完全溶解;
⑤培养基成分未充分混匀。
2、异常现象二:pH不正确
原因分析:
①制备过程中过度加热;
②水质不佳;
③外部化学物质污染;
④测定pH时温度不正确;
⑤pH计未正确校准;
⑥脱水培养基质量差。
3、异常现象三:颜色异常
原因分析:
①制备过程中过度加热;
②水质不佳;
③pH不正确;
④外来污染;
⑤脱水培养基质量差。
4、异常现象四:产生沉淀
原因分析:
①制备过程中过度加热;
②水质不佳;
③脱水培养基质量差;
④pH计未正确控制。
5、异常现象五:培养基出现抑制/低的生长率
原因分析:
①制备过程中过度加热;
②脱水培养基质量差;
③水质不佳;
④使用成分不正确,如:成分称量不准,添加剂浓度不正确;
⑤制备容器或水中的有毒残留物。
6、异常现象六:选择性差
原因分析:
①制备过程中过度加热;
②脱水培养基质量差;
③配方使用不对;
④添加成分的加入不正确,例如加入添加成分时培养基过热或添加浓度错误;
⑤添加剂污染。
7、异常现象七:污染
原因分析:
①不适当的灭菌;
②无菌操作技术存在问题;
③添加剂污染。
六、实验过程
1、2016版平板法VRBA倾注完,待琼脂凝固后为什么需要加3-4mL的覆盖层?
A:因为大肠菌群是需氧及兼性厌氧的,再加一层琼脂相当于造就一个半厌氧环境,促进兼性厌氧菌的生长,同时抑制其他菌的生长。除此之外,还有防止菌落蔓延的作用,防止迁徙性菌落对菌落计数构成影响。例如一些变形杆菌就会有迁徙现象,从而导致菌落长成一片无法区分。在表面多覆盖一层培养基就可以避免这种情况的发生。
2、GB 4789.3-2016平板法验证菌落如何挑取?
A:分别计数平板上出现的典型和可疑大肠菌群菌落数。按比例挑取10个不同类型的典型和可疑菌落,少于10个菌落的挑取全部典型和可疑菌落。假如在1:10的平板上可疑大肠菌群有10个,典型大肠菌群有6个。证实实验应该按照可疑跟典型5:3的比例进行挑取,移种于BGLB肉汤管内。
七、结果处理
1、所有稀释度都不在计数范围内怎么办?
这种情况一般都是最低稀释度的平板都小于15CFU,这种情况就是以最低稀释度的平板菌落数乘以验证试验的比例来计算。例如10倍稀释的两个平板上菌落数分别为10、8,菌落数为10的平皿挑取10个菌落复发酵中有8个菌落产气,菌落数为8的平皿挑取8个菌落复发酵中有7个菌落产气,则计算过程是这样的:(10*8/10+8*7/8)/2*10=75CFU/g(mL)。
2、连续两个稀释度的四个平皿的菌落数都在计数范围内怎么办?
这个需要参考菌落总数检测国标里7.1.2里的公式计算。我们需要先计算每个平皿的验证后的菌落数,再代入公式计算即可。例如10倍稀释度两个平皿菌落数为120和125,100倍稀释度两个平皿的菌落数为17和16,经过复发酵验证产气的管数分别为7、8、8、8,则我们先计算每个平皿上的菌落数分别为120*7/10=84,125*8/10=100,17*8/10=13.6(我们计14),16*8/10=12.8(我们计13),然后将84、100、14、13四个数代入公式:(84+100+14+13)/(2+0.2)*10=959,结果应报告960CFU/g(mL)。
3、只有一个稀释度的一个平皿的菌落数在计数范围,其他均不在计数范围怎么办?
这样我们只需要复发酵验证这一个平皿即可,根据这一个平皿的菌落数进行报告。例如10倍稀释度两个平皿菌落数为160和142,100倍稀释度两个平皿的菌落数为12和13,则我们只需要从菌落数为142CFU的平皿里挑取10个菌落进行复发酵验证即可,假如共有7支发酵管阳性,则应计算142*7/10=99.4,结果报告990CFU/g(mL)。
注意:对于结果检出的平板或试管需要经过无害化处理(121℃灭菌30分钟)方能弃去,防止对环境造成污染。














 当前所在页面:
当前所在页面: